化妝品新政88號文出臺,使近年的化妝品市場充滿活力,眾多國內品牌與國外品牌化妝品紛紛進入中國消費者的視野。據調查對于消費者而言,70%以上的客戶希望了解化妝品原料的功效信息;對于化妝品廠商而言,安全無毒而又新穎的原料是產品宣傳的傳統“亮點”。在化妝品研發之初,需要首先判斷化妝品原料是否可以合規添加,如果未來計劃在華銷售,某些不可或缺的原料成分卻尚未列入中國的化妝品可使用原料清單,這樣的產品即使研發出來,也是不允許在華銷售的,需要先完成化妝品新原料的申報才能進行成品的申報。
所以在此為大家介紹一下中國化妝品新原料行政許可申報的相關法規、申報流程以及近年來的法規趨勢,以讓更多的業內人士了解情況,將更多更好的原料在中國實現合規申報,合法銷售和使用。
化妝品新原料定義與申請人
化妝品新原料是指國內首次使用于化妝品生產的天然或人工原料。
國產化妝品新原料行政許可申請人應是化妝品原料生產企業或化妝品生產企業;進口化妝品新原料行政許可申請人應是進口化妝品新原料生產企業或化妝品生產企業。
主管當局
決定機構:國家藥品監督管理局
受理機構:國家藥品監督管理局保健食品審評中心
其他相關機構:
中國環境保護部:監管在中國境內生產或進口銷售新化學物質,含化妝品原料或中間體;海關和出入境檢驗檢疫局:進出口清關檢驗檢疫。
相關法規
《化妝品新原料申報與審評指南》、
《化妝品衛生監督條例》、
《化妝品衛生監督條例實施細則》、
《健康相關產品衛生行政許可程序》、
《化妝品行政許可申報受理規定》、
《化妝品行政許可受理審查要點》、
《化妝品新原料審批服務指南》
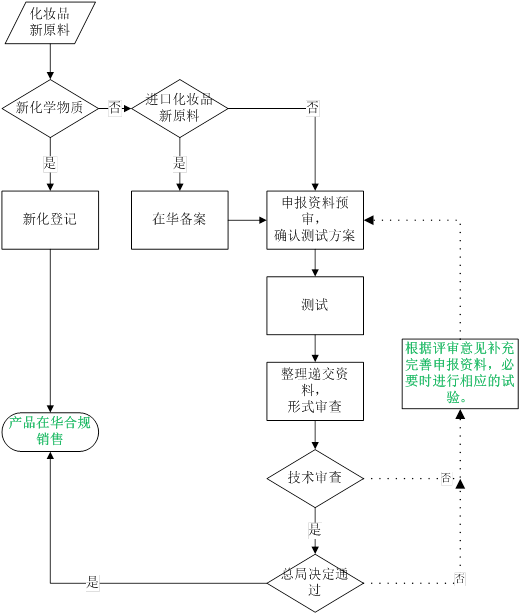
登記流程
化妝品新原料行政許可申報資料要求
1)化妝品新原料行政許可申請表;
2)研制報告;
3)生產工藝簡述及簡圖;
4)原料質量安全控制要求;
5)毒理學安全性評價資料(包括原料中可能存在安全性風險物質的有關安全性評估資料);
6)進口化妝品新原料申請人,應提交已經備案的行政許可在華申報責任單位授權書復印件及行政許可在華申報責任單位營業執照復印件并加蓋公章;
7)可能有助于行政許可的其他資料。另附送審樣品1件。
未來趨勢
近年來批準的化妝品新原料屈指可數。我國對化妝品原料采取嚴格的管理措施,這與美國和歐盟等大部分發達國家類似。在現今化妝品新原料管理體系下,化妝品新原料注冊難度大、周期長。企業若使用未經批準的化妝品新原料責任較大:依據情節輕重,會處違法所得的3到10倍罰款,或5年內不受理相關責任人及企業提出的化妝品許可申請。
2014年開始,CFDA不再發布化妝品新原料審批公告,而是向批準的化妝品新原料申請人發放《化妝品新原料試用批件》,批件設立一定有效期。核準范圍以外的其它企業如需使用該原料生產化妝品必須另行向CFDA申報。首先申請批件的企業一旦通過審批,可以利用保護期在競爭激烈的化妝品市場上獲得先機。
2018年為進一步做好化妝品注冊備案管理工作,國家藥監局對美國個人護理產品協會(PCPC)出版的《國際化妝品原料字典和手冊(第16版)》(International Cosmetic Ingredient Dictionary and Handbook(2016 Sixteenth Edition))進行翻譯,形成了《國際化妝品標準中文名稱目錄(2018版)(征求意見稿)》,此意見稿包括22620種物質;此目錄的更新有利于全球化妝品及原料成分標識信息的統一,也能看出中國化妝品新原料的品種數(目前只有8783種)有很大的上升空間。但根據當前中國化妝品法規要求,企業仍需要依據IECIC(2015)目錄中的8783個成分判斷是否屬于化妝品新原料。
推測化妝品新原料未來幾年會有如下的趨勢:數量上會有一定的新增;審批制度方面預計會根據產品安全評估難度的不同級別給予分類管理,使更多的好的原料盡快通過申報;監管制度方面預計會建立相對完善的新原料追溯制度和安全風險信息搜集制度,政府機構加大事中事后監管職能,讓企業更好的為產品質量安全負責。